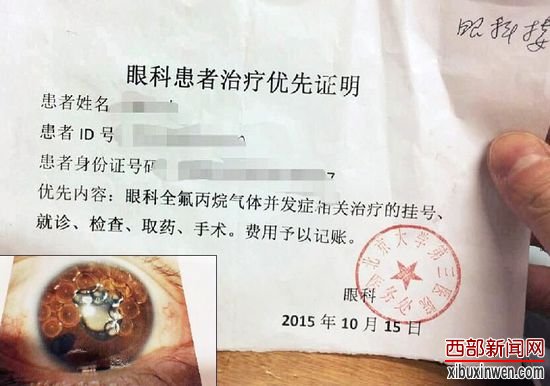
图为北医三院给发生不良反应的患者提供的优先挂号和复查证明。小图为患者王明(化名)术后右眼发生不良反应,医院将其眼中的气体抽出后,重新注入硅油。患者供图
法制晚报讯(记者 张丽 张群琛 陈威)“问题医用气体致盲”事件中,患者所使用的眼用全氟丙烷气体,生产厂商为天津晶明新技术开发有限公司。
今天上午,该公司负责人雷先生告诉《法制晚报》(微信公号ID:fzwb_52165216)记者,目前所涉及的两个批次的药品已经全部召回,事发后公司也组织了自查,“目前主要的工作还是配合国家的调查和积极应对后续的司法程序。”
涉事企业 将积极应对后续的司法程序
天津晶明新技术开发有限公司官网介绍,该公司为中国唯一眼表检测及眼科耗材品研发生产基地。2014年9月5日,该公司获得国家食药监总局颁发的医疗器械注册证,准许该公司生产的眼用全氟丙烷气体入市,有效期至2019年9月4日。
2015年10月23日,国家卫生计生委办公厅曾针对天津晶明新技术开发有限公司生产的眼用全氟丙烷气体可疑群体不良事件作出后续处理情况的通报。
通报指出,2015年6月,天津晶明新技术开发有限公司生产的眼用全氟丙烷气体在北京、江苏两地发生可疑群体不良事件,食品药品监管总局和国家卫生计生委印发通知,要求各地停止使用该公司生产的眼用全氟丙烷气体。
2015年7月,天津晶明新技术开发有限公司已完成对2015年生产的两个批次(生产批号为15040001、15040002)产品的召回工作。食品药品监管部门对北京和江苏两地涉事产品和企业召回产品按注册产品标准进行了检验,上述产品“含量”项目不符合标准规定,江苏涉事产品和企业召回产品“皮内反应”项目不符合标准规定。
“从去年7月份,发生此事之后,我们两个批次的药品已经全部召回,国家卫计委在去年10月份也已经进行了公告。” 天津晶明新技术开发有限公司负责人雷先生表示。
据了解,目前该企业生产的全氟丙烷气体的生产线仍处于停产状态,市场上并无该问题批次及相邻批次产品。
“外部,我们遵照国家的司法判定、法院的判决。内部,事情发生之后,我们就立即组织了自查,目前主要的工作还是配合国家的调查和积极应对后续的司法程序。”天津晶明新技术开发有限公司负责人雷先生表示。